Le laboratoire SABNP, sous tutelle de l’Université Évry Paris-Saclay et de l’Inserm, et labellisé Genopole, a découvert pourquoi, dans la maladie de Charcot, les agrégats pathologiques des neurones sont essentiellement constitués de la protéine TDP43, et comment l’agrégation s’opère. Ce phénomène d’agrégation propre à plusieurs maladies neurodégénératives est gouverné par le domaine N-terminal de TDP-43, une partie qui jusqu’à présent retenait peu l’attention des scientifiques et des industries pharmaceutiques. Cette découverte publiée le 21 janvier 2026 dans Nature Communications, ouvre une nouvelle piste thérapeutique pour cet enjeu majeur de santé public.
La sclérose latérale amyotrophique, connue aussi sous le nom de maladie de Charcot, et la dégénérescence fronto-temporale sont caractérisées par la présence dans les neurones des patients d’inclusions cytoplasmiques insolubles constituées de protéines agrégées.
Parmi ces protéines, TDP-43 est la plus fréquemment retrouvée : 97 % des patients atteints de la maladie de Charcot, dont des formes familiales dues à des mutations génétiques, présentent des agrégats de TDP-43
Pourquoi et comment la protéine TDP-43 s’agrège ?
TDP-43 est une protéine dite « de liaison à l’ARN ». En conditions normales, dans sa forme soluble, elle s’attache aux ARN messagers, molécules centrales de l’expression des gènes dans les cellules. Elles régulent ainsi leur épissage, leur transport ou leur stabilité.
Par sa prédominance dans la maladie de Charcot, TDP-43 retient l’attention des laboratoires pharmaceutiques en quête de cibles thérapeutiques. Mais pour que des pistes se précisent, des questions essentielles restent à élucider.
- Pourquoi les agrégats cellulaires observés dans la maladie de Charcot sont-ils majoritairement constitués de la protéine TDP-43 ?
- Quel mécanisme gouverne la transition de TDP-43 d’un état physiologiquement fonctionnel en un état agrégé toxique ?
Alors que les recherches se concentrent surtout sur les domaines de TDP-43 portant les mutations responsables de la maladie, les scientifiques évryens se sont intéressés à son domaine N-terminal (NTD), c’est-à-dire à la partie portant le groupe amine libre (-NH2) à une extrémité de la protéine. Le laboratoire SABNP (Structure et Activité des Biomolécules Normales et Pathologiques) est spécialiste de l’exploration structurale et fonctionnelle des interactions ARN/protéines et étudie leur rôle dans les cancers et les maladies neurodégénératives. En mettant en œuvre son expertise ainsi que les technologies dont il dispose sur la plateforme génopolitaine de Biologie structurale*, gérée par l’équipe, le laboratoire a révélé que les interactions entre domaines NTD favorisent le phénomène d’agrégation.
Le domaine NTD de TDP-43 : déclencheur de l’agrégation
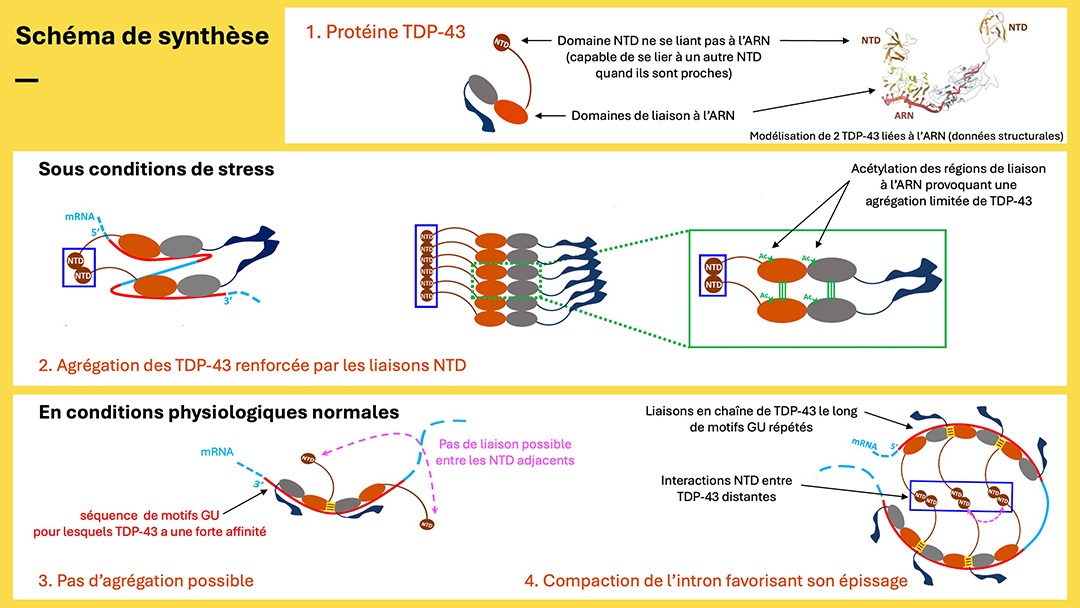
Le domaine NTD de TDP-43 présente une structure globulaire repliée qui ne se lie pas à l’ARN (cf. schéma de synthèse, point 1). Par ailleurs, ce domaine n’est connu jusqu’alors que pour sa capacité d’initier des interactions dites « homotypiques » (TDP-43/TDP-43). Aucune autre protéine de liaison à l’ARN ne possède un domaine NTD semblable. Le travail du laboratoire a permis d’élucider le rôle de ce domaine dans les fonctions physiologiques de TDP-43 et dans son agrégation pathologique.
Sous conditions de stress, tel un stress oxydant qui s’installe avec l’âge, TDP-43 subit une acétylation de ces régions de liaison à l’ARN qui favorise l’agrégation de TDP-43. Cependant, en l’absence d’interaction entre les domaines NTD, l’agrégation reste limitée. Le laboratoire génopolitain a montré que lorsque des interactions NTD/NTD prennent place de manière incontrôlée, la formation irréversible d’agrégats cytoplasmiques de TDP-43 devient dramatique (cf. schéma de synthèse).
La découverte par le laboratoire SABNP de cet effet pathologique de NTD explique pourquoi, en conditions de stress, TDP-43 est plus susceptible que les autres protéines de s’agréger, et donc sa prévalence dans les pathologies neurodégénératives comme la maladie de Charcot.
Un mécanisme pathologique, mais aussi physiologique mis au jour pour la première fois
Le laboratoire SABNP a aussi révélé que le domaine NTD joue un rôle majeur, en conditions physiologiques normales, dans la phase de maturation des ARN messagers produits par les neurones pour assurer leurs fonctions naturelles. Le mécanisme, démontré par l’analyse des interactions moléculaires à l’échelle atomique par spectrométrie RMN, se déroule comme suit.
La protéine TDP-43 se lie à de longues séquences d’acides ribonucléiques (A, U, G et C) de l’ARN avec une forte spécificité pour les motifs GU. L’occurrence de ces motifs est particulièrement marquée dans les introns présents dans les noyaux des neurones. Lorsque plusieurs protéines TDP-43 se fixent le long de séquences GU répétées, ces liaisons en chaîne imposent une contrainte géométrique qui maintient éloignés les domaines NTD des TDP-43 adjacents. Les NTD proches ne peuvent donc pas interagir, il y a alors peu de risque d’agrégation (cf. schéma de synthèse, point 3).
Les chercheurs sont allés plus loin en appliquant la méthode SAXS qui offre une vision plus large, à l’échelle du nanomètre (Small-Angle X-ray Scattering, ou diffusion des rayons X aux petits angles, en collaboration avec le Synchrotron Soleil). Ils ont montré que cet agencement, en laissant libres les NTD proches, contribue par contre à favoriser des interactions NTD/NTD entre molécules TDP-43 distantes le long de l’intron. Ces liaisons assurent alors la compaction de l’intron. Elles facilitent ainsi son épissage (cf. schéma de synthèse, point 4), c’est-à-dire la phase d’excision nécessaire pour que la séquence ARN soit traduite par la machinerie cellulaire en protéines neuronales fonctionnelles.
Ce mécanisme explique pourquoi la fonction physiologique de TDP-43 est particulièrement importante et pourquoi son agrégation est toxique pour les neurones.
Ces observations structurales ont été confirmées dans un contexte cellulaire par la méthode ‘’Microtubule Bench’’ de visualisation et quantification des interactions moléculaires dans les cellules vivantes, brevetée par le laboratoire SABNP (lire le communiqué de presse de 2015).