La fibrose radio-induite est un processus qui survient chez environ 30% des femmes dans les 10 années qui suivent une radiothérapie pour un cancer du sein.
Elle provoque généralement un durcissement, un changement d’apparence et une rétractation du sein, accompagnés d’une gêne ou d’une douleur.
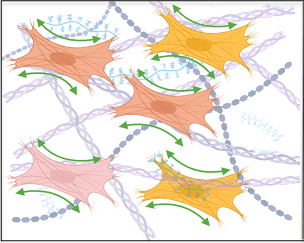 Ce processus physiopathologique correspond au remplacement progressif du tissu conjonctif fonctionnel par un tissu non fonctionnel fibreux. Le phénomène est dû à une dérégulation des processus de réparation associée à une activation incontrôlée des fibroblastes, qui se transforment en myofibroblastes fibrogènes. Ceux-ci produisent une matrice fibreuse pathologique, la contracte en un réseau resserré autour d’eux, formant ainsi un tissu modifié, de type cicatriciel (cf. visuel).
Ce processus physiopathologique correspond au remplacement progressif du tissu conjonctif fonctionnel par un tissu non fonctionnel fibreux. Le phénomène est dû à une dérégulation des processus de réparation associée à une activation incontrôlée des fibroblastes, qui se transforment en myofibroblastes fibrogènes. Ceux-ci produisent une matrice fibreuse pathologique, la contracte en un réseau resserré autour d’eux, formant ainsi un tissu modifié, de type cicatriciel (cf. visuel).
Compte tenu de l’impact physique et psychologique de cet effet indésirable de la radiothérapie, prédire le risque des patientes de développer une fibrose et progresser dans la compréhension du mécanisme constituent des attentes majeures.
Explorer le rôle des ARN non codants
Le rôle du TGFB1, un facteur de croissance qui active la transformation des fibroblastes en myoblastes lorsqu’il est présent à forte dose, a été établi dans la fibrose. Néanmoins, la recherche de facteurs génétiques n’a pas abouti pour l’instant à l’identification de biomarqueurs pertinents de la susceptibilité à la fibrose.
Le laboratoire LGRK (Laboratoire de génomique et radiobiologie de la kératinopoïèse, CEA-Université d’Évry Paris-Saclay) s’est intéressé aux ARN non codants, qui constituent actuellement un vaste champ d’exploration. Ces séquences d’ARN non traduites en protéines révèlent en effet des fonctions régulatrices majeures.
Publiée dans International Journal of Radiation Oncology, Biology, Physics, l’étude du laboratoire a porté sur des fibroblastes dermiques isolés de la peau non irradiée de patientes ayant ou non développé une fibrose mammaire sévère après radiothérapie. Les analyses ont porté sur le séquençage du transcriptome, c’est-à-dire l’ensemble des ARN de ces cellules, et sur leur analyse fonctionnelle.
VIM-AS1, biomarqueur de susceptibilité à la fibrose radio-induite
L’équipe du LGRK a ainsi identifié une signature de la susceptibilité à la fibrose mammaire comprenant 15 ARN longs non codants (lnc RNAs). Parmi eux, VIM-AS1 a été identifié comme potentiel biomarqueur associé au risque de fibrose.
Les scientifiques ont confirmé le rôle de ce lnc RNA comme effecteur du mécanisme fibrotique : lorsqu’ils le répriment par interférence ARN avec des oligonucléotides antisens, ils observent une baisse de la transition de fibroblastes sains en myofibroblastes inducteurs de fibrose.
De plus, en réprimant VIM-AS1, ils diminuent la contractilité importante des myofibroblastes, également observée dans les fibroses.
Les données démontrent l’implication de VIM-AS1 dans la transformation fibroblaste-myofibroblaste. En effet, dans les cellules, sa synthèse est corégulée avec l’expression du gène codant pour la vimentine.
Or, cette protéine filamenteuse, qui joue un rôle de chef d’orchestre dans le processus de cicatrisation, est régulée par TGFB1, effecteur principal de cette transformation.
Le laboratoire a d’ailleurs confirmé que TGFB1 induit aussi l’expression de VIM-AS1 dans les fibroblastes.
L’appui technologique de Genopole et de son écosystème
Des équipements financés par Genopole, à disposition sur deux plateformes technologiques installées au LGRK, ont servi aux expérimentations :
- la plateforme d’irradiation expérimentale, dotée d’un générateur de rayons X, utilisée ici pour étudier l’expression de VIM-AS1 en réponse à différentes doses de radiations, ainsi que d’un équipement de PCR digitale pour la quantification des ARN dans les échantillons de fibroblastes.
- La plateforme de cytométrie constituée notamment d’un cytomètre-analyseur pour l’étude fonctionnelle des fibroblastes. Elle fait partie du réseau génopolitain de plateformes d’imagerie-cytométrie OCCIGEN
Le LGRK a bénéficié pour cette étude de la plateforme de séquençage et de l’expertise en génomique du CNRGH (Centre national de recherche en génomique humaine, CEA), également installé sur le biocluster évryen.
Du facteur moléculaire au développement thérapeutique : l’étude ouvre des perspectives translationnelles au LGRK
Par ces travaux, le LGRK a identifié non seulement un biomarqueur de susceptibilité à la fibrose mammaire radio-induite, mais aussi, compte tenu de l’implication de VIM-AS1 dans une étape clé du processus fibrotique, une cible potentielle pour des traitements préventifs ou curatifs.
Plus largement, le laboratoire génopolitain a démontré l’intérêt d’examiner le vaste champ des ARN non codants, encore balbutiant, pour décortiquer les processus pathologiques dus à divers stress tels que l’exposition au soleil ou à des substances, le vieillissement, etc.

 Nicolas Fortunel, directeur du
Nicolas Fortunel, directeur du